Неінвазивний аналіз крові для оцінки стану слизової оболонки шлунка, виявлення атрофічного гастриту та інфекції Helicobacter pylori без проведення гастроскопії.

Запальні зміни слизової оболонки шлунка, зокрема атрофічний гастрит, є частою причиною гострих шлунково-кишкових розладів і болю у верхній частині живота. Хронічне запалення може супроводжуватися такими симптомами, як метеоризм, втрата апетиту, здуття живота та печія, однак у багатьох випадках перебігає без виражених проявів. За відсутності лікування атрофічний гастрит може призвести до серйозних ускладнень. Так, з невеликих ділянок запалення можуть розвиватися виразки шлунка або дванадцятипалої кишки. Крім того, в атрофічно зміненій слизовій оболонці можуть виникати метапластичні зміни, що підвищує ризик розвитку раку шлунка. Сьогодні гастроскопія є надійним методом діагностики атрофічного гастриту, однак це інвазивна процедура, яка має певні протипоказання та обмеження.
GastroPanel® – це неінвазивний аналіз крові, що дозволяє оцінити структуру та функціональний стан слизової оболонки шлунка з урахуванням можливої інфекції Helicobacter pylori. Дослідження ґрунтується на визначенні специфічних біомаркерів шлунка — пепсиногену I та II, а також гастрину-17. Завдяки цьому тест допомагає виявити атрофічний гастрит і визначити його локалізацію (у тілі або антральному відділі шлунка). Використання GastroPanel® як скринінгового методу дозволяє точніше визначити групу пацієнтів, яким дійсно необхідно пройти гастроскопію. Якщо результати тесту є негативними за всіма показниками у пацієнтів із симптомами, причиною скарг може бути функціональна диспепсія (так званий «подразливий шлунок») або інше захворювання, не пов’язане зі слизовою оболонкою шлунка, і проведення гастроскопії не завжди є обов’язковим.
Водночас, враховуючи те, що хронічний атрофічний гастрит часто перебігає безсимптомно, тест може допомогти виявити людей, які не мають скарг, але у яких результати дослідження свідчать про атрофічні зміни слизової оболонки шлунка. У таких випадках проведення гастроскопії може бути доцільним для подальшої діагностики.
Про типи гастриту і чим вони відрізняються читайте у статті «Класифікація гастритів».
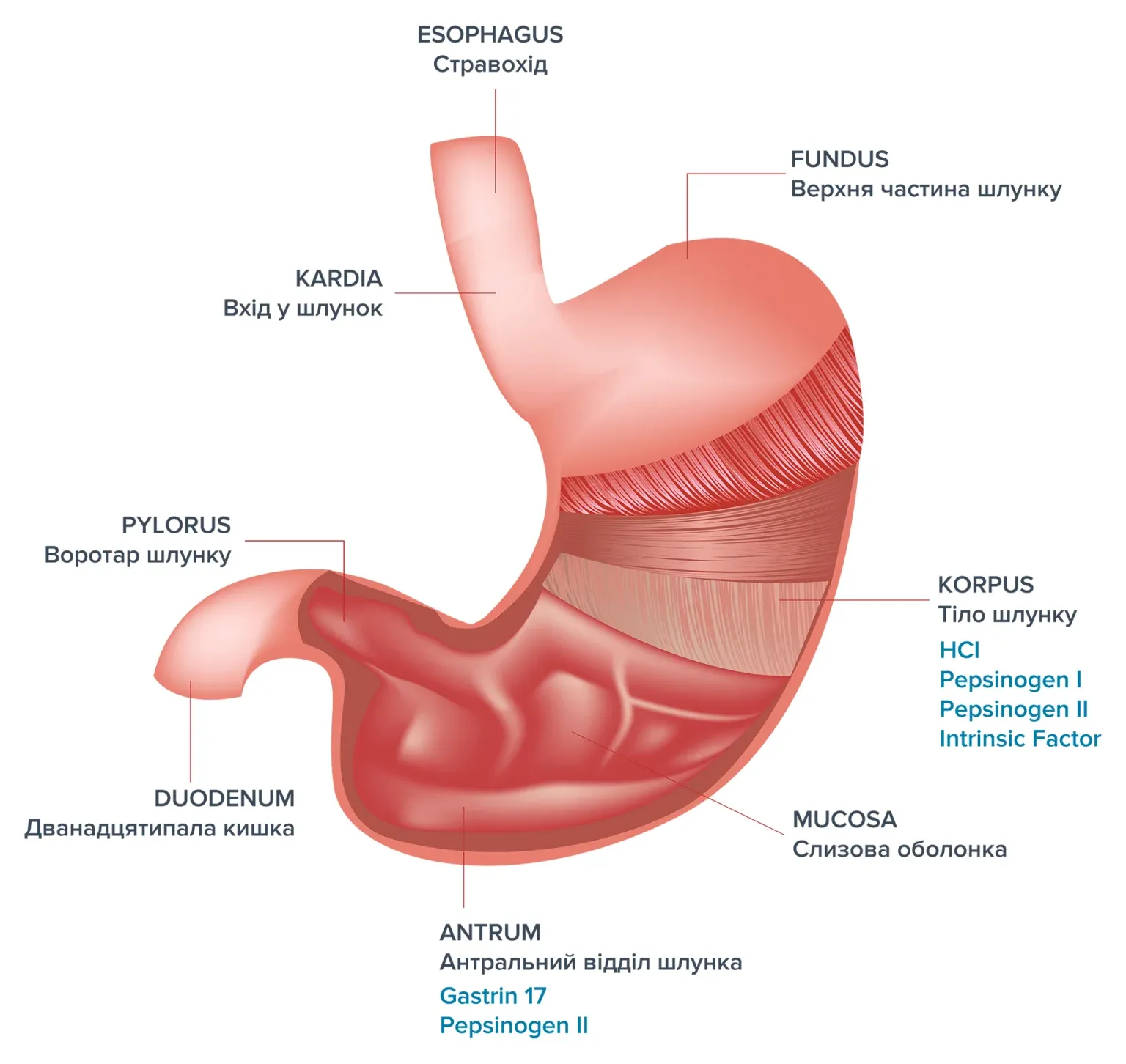
Шлунок можна умовно розділити на наступні відділи:
Стравохід відкривається у верхню частину шлунка — дно (Fundus). Основну частину органа становить тіло шлунка (Corpus). У ділянці виходу зі шлунка розташований антральний відділ (Antrum), який переходить у пілорус (Pylorus, воротар шлунка) — структуру, що з’єднує шлунок із дванадцятипалою кишкою (Duodenum).
Шлунок виконує ряд важливих завдань для ефективного перетравлення поживних речовин у кишківнику. Після того як їжа подрібнюється в ротовій порожнині та змішується зі слиною, у шлунку до харчової маси додаються додаткові травні ферменти — часто у вигляді неактивних попередників (наприклад, пепсиногени). Завдяки перистальтичним рухам шлунка харчова маса ретельно перемішується і набуває однорідної консистенції. Оскільки протеолітичні ферменти найефективніше працюють у кислому середовищі, вміст шлунка підкислюється соляною кислотою (HCl).
Багато харчових компонентів (білки та клітковина) є складними молекулами й тому важко перетравлюються. Завдяки індукованій кислотою денатурації (руйнуванню третинної структури) цих молекул, створюються кращі можливості для ферментативного травлення. Секреція шлункового соку також має дезінфекційну дію. Більшість патогенів, таких як бактерії, віруси та інші мікроорганізми, знищуються низьким значенням pH. Крім того, до харчової суміші в шлунку додається специфічний транспортний глікопротеїн — внутрішній фактор (Intrinsic Factor) для ефективного всмоктування вітаміну В12 з їжі в кишківнику.
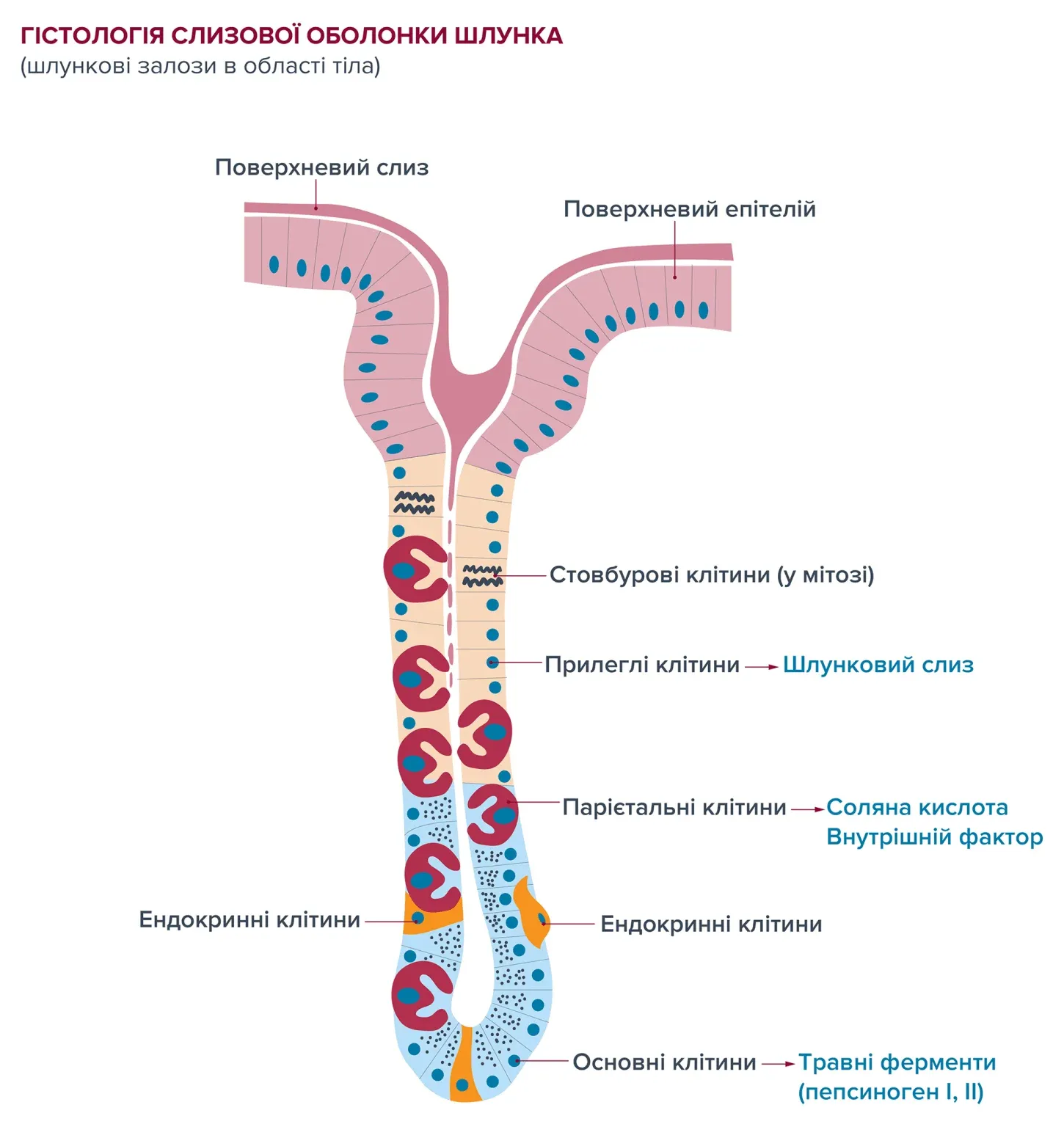
Стінка шлунку складається з багатьох шарів. У слизовій оболонці шлунку, внутрішньому шарі органу, є шлункові залози, які складаються з різних типів клітин і відкриваються в просвіт шлунку. Секреція шлункового соку основними клітинами (травні ферменти) та парієтальними клітинами (соляна кислота, внутрішній фактор), а також вироблення шлункового слизу вторинними клітинами відбувається головним чином у слизовій оболонці тіла та дна шлунку. Слиз, яка покриває слизову оболонку тонкою плівкою, служить насамперед для захисту шлунку від самоперетравлення агресивним шлунковим соком і для захисту від патогенних мікроорганізмів. Кількість шлункового соку або шлункової кислоти, що виділяється залежить від виду та кількості споживаної їжі. Деякі харчові продукти (наприклад, кава, нікотин, спеції), зокрема, стимулюють утворення кислоти.
Слизова оболонка шлунку, кровообіг та імунний захист утворюють функціональну одиницю, яка називається бар’єром слизової оболонки. Слизова оболонка перебуває в постійній трансформації (нарощуванні та руйнуванні клітин) і зазвичай швидко відновлюється після пошкодження. Але якщо функція порушена або послаблення чи пошкодження занадто сильні, це може призвести до запалення слизової оболонки.
Кожен, хто неодноразово або постійно страждав такими симптомами, як біль у шлунку, нудота або проблеми з травленням, повинен бути обстежений як можливо раніше. Якщо у вас є кров у калі або у блювоті, слід негайно звернутися до лікаря. Ретельний анамнез та ретельне фізичне обстеження (наприклад, ультразвукове дослідження) іноді можуть надати достатньо доказів гастриту. Однак, надійний діагноз можливий лише за допомогою гастроскопії.
Для пацієнтів, які хочуть уникнути незручностей під час проведення гастроскопії, або для яких таке втручання може бути тягарем через їх вік, неінвазивна діагностика є бажаною альтернативою для перевірки показань для проведення гастроскопії.
Це також стосується пацієнтів, яким гастроскопія не може бути проведена через анатомічні особливості. GastroPanel®- доступний аналіз крові, за допомогою якого можна перевірити підозрюваний діагноз атрофічного гастриту та визначити можливу локалізацію запалення слизової шлунку.
Перевага цього аналізу крові полягає в тому, що він не є стресовим, а отже, може бути використаний і для профілактичного медичного огляду у літніх людей. GastroPanel® був підтверджений у кількох великих дослідженнях, заснованих на гастроскопії, підтверджених біопсією. Усі дослідження були включені у відповідний метааналіз.
В рамках аналізу крові GastroPanel® для оцінки структури та функції слизової шлунку визначають концентрацію чотирьох різних параметрів у плазмі крові за допомогою кількісного імуноферментного тесту (ІФА):
За результатами можна зробити твердження про наявність інфекції в минулому або активної інфекції H. pylori, що є необхідною умовою для більшості випадків гастриту. Крім того, результати GastroPanel® можуть підтвердити існування атрофічного гастриту та локалізацію запального пошкодження слизової оболонки (тіла, антрального відділу).
H.pylori – це спіралеподібна, грамнегативна бактерія, яка колонізує шлунок у людини. Цей мікроорганізм осідає в слизовій оболонці на шлунковому епітелії та в залозах, але, здається, не проникає в клітини епітелію. Інфекція H. pylori є найпоширенішою причиною хронічного гастриту, оскільки слизова оболонка навколо областей, де колонізується бактерія, завжди запалюється. Цей стан відомий як хронічний поверхневий гастрит або неатрофічний гастрит, який триває все життя, якщо його не лікувати. Без успішного знищення бактерій цей хронічний запальний процес може призвести до атрофічного гастриту.
Більшість людей, які заражаються H. pylori, виробляють антитіла IgG до збудника. Вікова частота антитіл однакова у чоловіків та жінок. Багато пацієнтів з високим титром антитіл не мають симптомів, навіть якщо вони інфіковані H. pylori. Тому рівень антитіл не обов’язково корелює з тяжкістю клінічних симптомів. Якщо титр антитіл є єдиним визначеним біомаркером у GastroPanel®, який є підвищеним, це означає поверхневий, але не атрофічний гастрит, асоційований з H. pylori, в той час, як підвищений рівень антитіл, пов’язаний з аномаліями інших трьох біомаркерів, підтверджує діагноз атрофічного гастриту, асоційованого з H. pylori.
Проведення кількісного визначення антитіл людини класу IgG за допомогою ІФА для виявлення активної колонізації слизової шлунку має перевагу перед іншими загальноприйнятими методами аналізу (наприклад, дихальний тест з сечовиною 13С, тест калу на антиген): позитивних хворих на H. pylori можна вірогідно виявити також при наявності атрофічного гастриту, MALT-лімфоми, виразки шлунку або дванадцятипалої кишки, а також у людей, які приймають інгібітори протонної помпи або антибіотики.
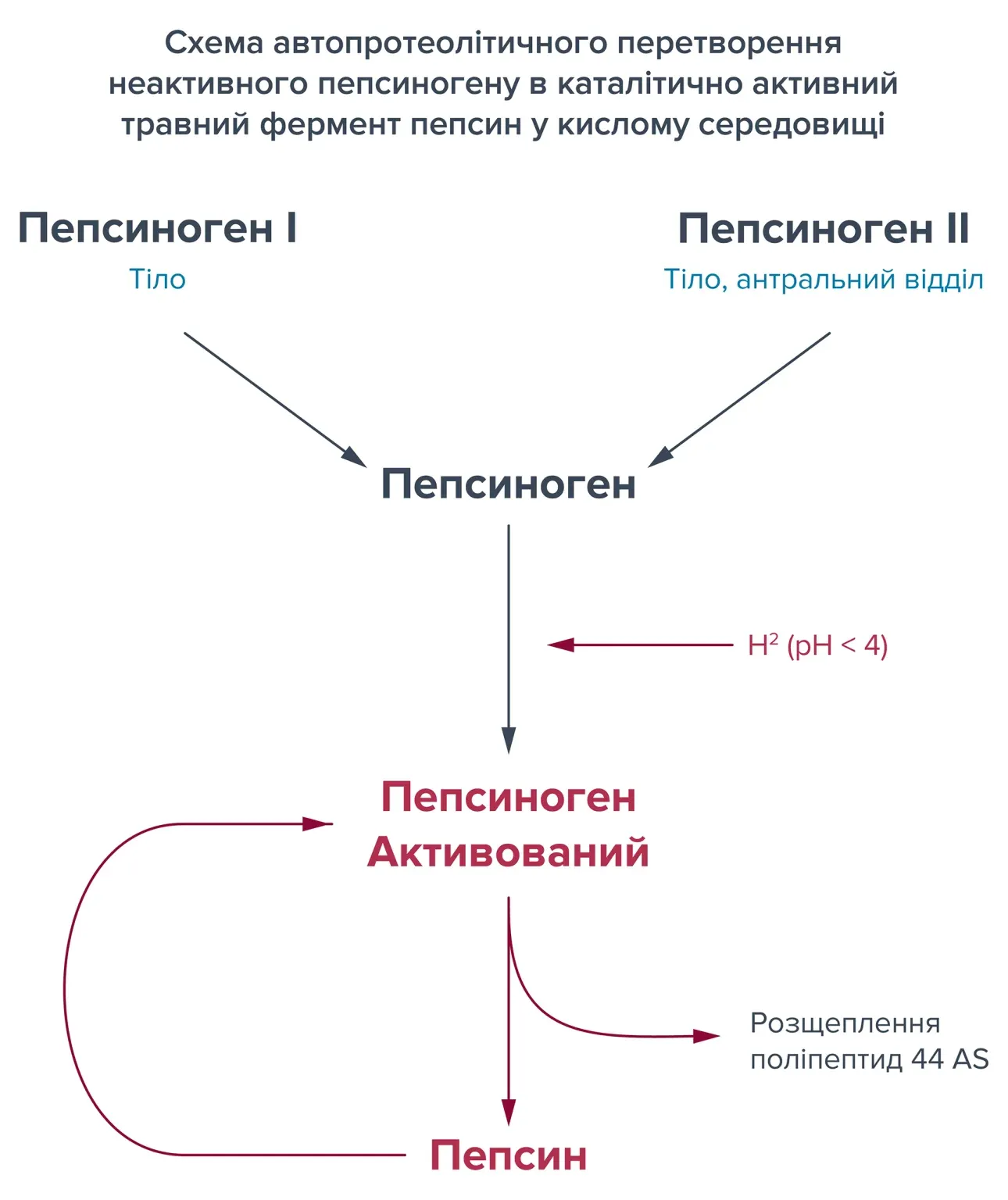
Пепсиногени I й II є неактивними попередниками (зимогенами) травного ферменту пепсину. Перетворення в каталітично активний фермент відбувається в кислому середовищі шлунку шляхом відщеплення довшої послідовності амінокислот (автопротеоліз). У той час, як пепсиноген I вивільняється в просвіт шлунку лише основними та вторинними клітинами тіла, пепсиноген II також виробляється пілоричними залозами антрального відділу та дванадцятипалої кишки.
Частина синтезованого пепсиногену I також виділяється в кров. Концентрація пепсиногену I у кровотоку корелює з кількістю основних клітин у слизовій оболонці тіла. Зменшення цих клітин, спричинене атрофією слизової, також призводить до лінійного зниження рівня пепсиногену I у плазмі крові. Низька концентрація (нижче норми) пепсиногену I у плазмі, таким чином, вказує на атрофічний гастрит тіла. Оскільки атрофічний гастрит у шлунковому тілі є значним фактором ризику раку шлунку, скринінг, через виявлення пепсиногену I, також може бути використаний для ідентифікації людей, які мають підвищений ризик новоутворення і повинні бути більш детально обстежені за допомогою гастроскопії.
Підвищений рівень пепсиногену II у плазмі вказує на неатрофічне запалення слизової оболонки, яке зазвичай спричинене або інфекцією H. pylori, або тривалим вживанням препаратів ІПП. Вимірювання пепсиногену II також проводиться для одночасного використання з тестом на пепсиноген I для визначення співвідношення концентрацій пепсиногену I та II у плазмі (співвідношення ПГІ: ПГІІ). Співвідношення ПГІ: ПГІI виявилося ще одним важливим прогностичним параметром для оцінки структури та функції слизової шлунку. Якщо співвідношення, яке зазвичай становить від 3 до 20, опускається нижче норми, ймовірний атрофічний гастрит від помірного до важкого ступеня, а ризик розвитку раку шлунка значно збільшується.
Гастрини – це лінійні пептидні гормони, які виробляються так званими G-клітинами в антральному відділі шлунку, а також у дванадцятипалій кишці та підшлунковій залозі, і звідти вони транспортуються по кровоносним судинам до місць дії. G-клітини вивільняють у кровотік суміш гастринів різної молекулярної ваги та різної довжини пептидів, які синтезуються з препрогастрину в результаті посттрансляційних модифікацій. У здорових людей переважною формою гастрину в плазмі / сироватці є амідований гастрин-17 (із 17 амінокислотами).
Утворення антитіл IgG може тривати кілька тижнів після фактичного зараження. Через персистентність антитіл і, як наслідок, затримку зменшення титру IgG у сироватці крові, тест ще короткий час може давати (помилково) позитивні результати, попри успішну ерадикацію інфекції H. Pylori. Отже, будь-яка ерадикація повинна враховуватися при інтерпретації результатів GastroPanel®.
Секреція гастрину контролюється постгангліонарними парасимпатичними нервовими волокнами блукаючого нерва (Nervus vagus) та нейронами ентеральної нервової системи, які індукують вивільнення нейроендокринними клітинами шлунку гормону гастрин-релізінг пептиду (GRP, Gastrin-Releasing-Peptide) стимулюючого G-клітинами. Механічне розтягування слизової оболонки антрального відділу, спричинене хімусом у шлунку, також призводить до утворення гастрину, особливо якщо хімус дуже багатий білками. Вживання алкоголю, кофеїну або нікотину також має стимулюючий ефект на G-клітини.
Основна функція гастринів – стимулювати секрецію шлункової кислоти парієтальними клітинами в шлунковому тілі та посилювати рухливість антрального відділу через гладкі м’язи. Крім того, гастрини стимулюють основні клітини шлунку до секреції пепсиногену I та II. Нормальні рівні гастрину-17 в плазмі вказують на нормальну структуру та функцію антрального відділу. Гастрин-17 також можна оцінити як непрямий біомаркер стану в шлунковому тілі, оскільки низькі або високі значення гастрину-17 можуть призвести до порушення функції тіла через негативну зворотну реакцію, викликану пептидним гормоном.
Результати GastroPanel® мають максимальну інформативну цінність, якщо визначення гастрину-17 проводиться окремо натщесерце і додатково після того, як секреція гастрину стимулюється прийняттям висококалорійного білкового напою. Наприклад, у пацієнтів з інфекцією H. pylori, у яких знижений базальний рівень гастрину-17, додаткове визначення рівня гастрину-17 після стимуляції може надати інформацію про те, чи має місце атрофічна слизова оболонка антрального відділу та чи виснажені G-клітини (рівень гастрину-17 залишається низьким після стимуляції) або чи слизова в антральному відділі непошкоджена, та чи виробляється занадто багато кислоти (рівень гастрину-17 значно зростав після стимуляції) у тілі через функціональний розлад антрального відділу?
Підвищений базальний рівень гастрину-17 у сироватці/плазмі також можна виміряти при рідкісній формі особливої неоплазії, гастриномі (захворюваність: 0,5-3 випадки / на 1 мільйон населення / на рік). Ця пухлина, яка диференціюється від клітин, що продукують гастрин, здебільшого розташована в підшлунковій залозі, рідше у дванадцятипалій кишці або шлунку. Постійна секреція гастрину, як правило, призводить до діареї та збільшення вироблення кислоти в шлунку, а отже, до розвитку повторних виразок у шлунку та дванадцятипалій кишці (синдром Золлінгера-Еллісона).
Тест GastroPanel® призначений для діагностики симптоматичних (диспептичних) дорослих пацієнтів. Якщо обстеження GastroPanel® виявляє негативний результат у пацієнтів із симптомами, існує велика ймовірність того, що шлункові симптоми спричинені функціональною диспепсією або захворюванням, незалежним від слизової шлунку. Крім того, скринінг безсимптомних осіб можливий для визначення груп ризику раку шлунку, в першу чергу пацієнтів з інфекцією H. pylori та атрофічним гастритом. Однак пацієнтам, у яких діагностували атрофію слизової оболонки шлунку за допомогою GastroPanel®, все ще потрібна гастроскопія, і вони повинні її пройти, щоб можна було додатково дослідити ступінь пошкодження слизової та виявити наявність можливих передпухлинних змін.
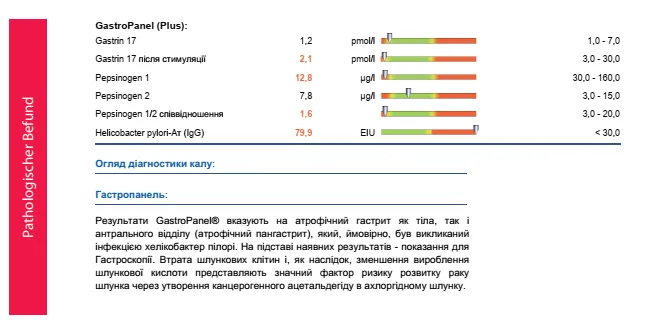
Референтні області GastroPanel®
IgG H. pylori (антитіла до Hp): <30 EIU
Пепсиноген I: 30-160 мкг/л
Пепсиноген II: 3 -15 мкг/л
Співвідношення PGI: PGII: 3-20
Гастрин-17, базальний: 1-7 пмоль/л
Гастрин-17, стимульований: 3-30 пмоль/л
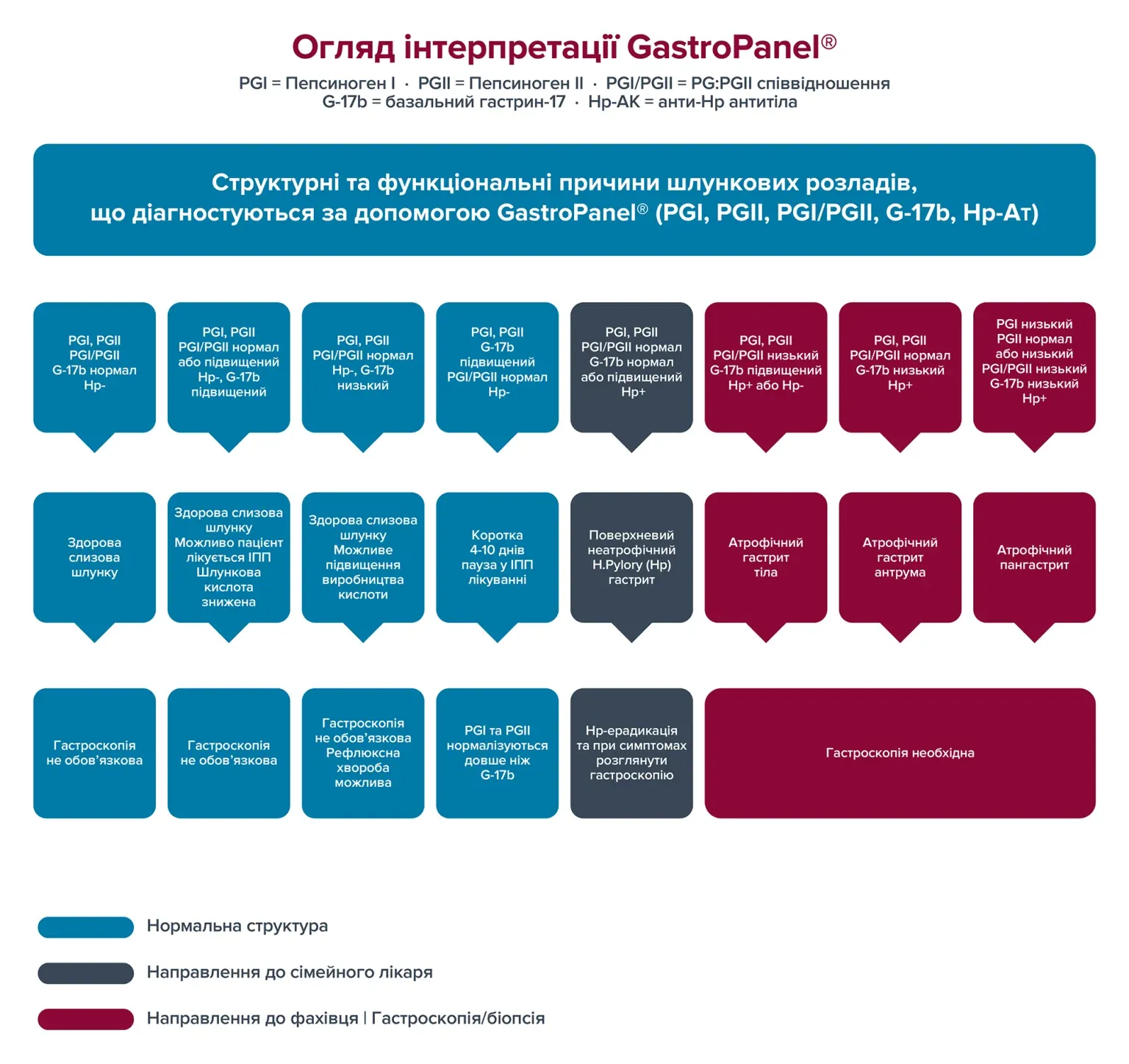
Тест GastroPanel® оптимізований для використання з оновленою Сіднейською системою класифікації гастриту 1 і в цьому сенсі розрізняють п’ять діагностичних класів на основі оцінки рівнів усіх чотирьох біомаркерів у плазмі крові:
1) нормальна слизова оболонка;
2) поверхневий (неатрофічний) H. pylori – асоційований гастрит;
3) атрофічний гастрит в антральному відділі;
4) атрофічний гастрит тіла;
5) атрофічний гастрит, як в антральному відділі, так і в тілі (пангастрит).
На додаток до цих п’яти категорій, які стосуються можливого пошкодження слизової шлунка, з результатів GastroPanel® можна отримати ще три специфічні діагностичні категорії для деяких функціональних розладів із нормальною морфологією шлунка.
Для проведення обстеження GastroPanel® необхідно замовити спеціальний набір тестів.
Першу пробу крові за допомогою пробірки ЕДТА беруть натщесерце, якщо це можливо, через десять годин (але принаймні хоча б чотири години) після утримання від їжі, кави та паління. Для визначення рівня гастрину-17 після стимуляції також беруть другу пробу крові після їжі. Для цього пацієнт приймає білковий порошок, що міститься в тестовому наборі, як напій. Через двадцять хвилин після споживання білкового напою кров відбирається в окрему пробірку ЕДТА.
Плазму слід відокремлювати негайно, але не пізніше як через дві години після забору крові, центрифугуванням пробірки ЕДТА. У виняткових випадках плазму також можна отримати без центрифугування, обережно осадивши клітинні компоненти проби крові та відокремивши їх від плазми.
Для виправляння проби використовують тільки нейтральні пробірки, передбачені в тестовому наборі, оскільки вони містять рідину-стабілізатор (GastroPanel® Stabilizer), яка гарантує стабільність зразка з урахуванням вимірюваних параметрів (особливо гастрину-17) під час транспортування до лабораторії. Доставлення має відбуватися протягом трьох днів при кімнатній температурі.
Щоб отримати повну інтерпретацію результатів GastroPanel®, під час виправляння проби слід заповнити спеціальну форму з даними анамнезу, давши відповідь на кілька питань (лікування, симптоми, прийняття ліків).


У випадках, коли через результати GastroPanel® виявлений аутоімунний гастрит (гастрит типу А) як можлива причина скарг пацієнта (наприклад, низький рівень пепсиногену I та відсутність антитіл до Hp), для виявлення/ виключення цієї форми хронічного атрофічного гастриту можна перевірити наявність (ауто) антитіл до парієтальних клітин (PCA) та/або внутрішнього фактора (IFA) у сироватці крові.
Цільовим антигеном РСА у парієтальних клітинах є насамперед Н+/ К+ -АТФ-аза, яка як протонна помпа бере значну участь в утворенні соляної кислоти у тілі шлунка. Діагностична чутливість PCA для аутоімунного гастриту становить від 80 до 90 %. У міру прогресування захворювання поширеність PCA зменшується в результаті втрати парієтальних клітин. Навіть у понад 90 % пацієнтів із перниціозною анемією в сироватці крові можна виявити циркуляційні аутоантитіла до парієтальних клітин.
Однак, PCA також виявляються у пацієнтів з аутоімунними ендокринопатіями (наприклад, тиреоїдит Хашимото, хвороба Аддісона, цукровий діабет 1 типу тощо), а також у здорових людей.
Антитіла до внутрішнього фактора (IFA) можуть бути виявлений приблизно у 50-70 % пацієнтів з аутоімунним гастритом і вважаються надзвичайно специфічними для хронічного атрофічного гастриту та пов’язаних із ним синдромів дефіциту вітаміну В12. У деяких пацієнтів без клінічних ознак перниціозної анемії можливо присутні антитіла до внутрішнього фактора (IFA). Однак у цих пацієнтів частіше клінічні прояви розвиваються у наступні роки.
Діагностичне значення присутності аутоімунного гастриту збільшується за рахунок комбінованого виявлення PCA та IFA, оскільки принаймні одне аутоантитіло виявляється приблизно у 90% уражених. Клінічні дослідження підтвердили хорошу кореляцію між виявленням антитіл та ендоскопічними результатами.
Антитіла до парієтальних клітин (PCA)
Антитіла до внутрішнього фактора (IFA)
У процесі аутоімунного гастриту руйнування парієтальних клітин часто призводить до суттєво зниженого вивільнення внутрішнього фактора, транспортного білка, необхідного для всмоктування вітаміну В12 в тонкому кишківнику. Якщо є підозра на гастрит типу А, слід визначати як запобіжний захід для злоякісної анемії рівень вітаміну В12 у сироватці крові. Якщо спостерігається дефіцит вітаміну В12, симптоми цієї форми анемії можна лікувати шляхом парентерального заміщення вітаміну В12.
Вітамін В12 у сироватці